ATRESIA
PULMONAR Y COMUNICACIÓN INTERVENTRICULAR ASOCIADA A ENDOCARDITIS INFECCIOSA
PULMONARY ATRESIA AND
VENTRICULAR SEPTAL DEFECT ASSOCIATED WITH INFECTIVE ENDOCARDITIS
Juan Sebastián Theran León ![]() 0000-0003-2192-7780,1 Germán Omar Díaz
Buitrago
0000-0003-2192-7780,1 Germán Omar Díaz
Buitrago ![]() 0000-0001-6943-901X,2 Marya Camila Rinaldy
Trujillo
0000-0001-6943-901X,2 Marya Camila Rinaldy
Trujillo ![]() 0000-0003-1671-19932
0000-0003-1671-19932
1 Médico residente de
medicina familiar de la Universidad de Santander, Bucaramanga, Colombia.
2 Médico interno de la Universidad de Santander, Bucaramanga.
AUTOR
PARA CORRESPONDENCIA
Juan Sebastián Theran León. Correo electrónico:
jtheran554@unab.edu.co
Los autores manifiestan no poseer conflictos de
intereses.
Resumen
Se presenta el caso de una paciente de 33 años
con antecedente de cardiopatía congénita tipo atresia pulmonar y ausencia del
sexto arco aórtico, comunicación interventricular, quien se encuentra
hospitalizada por endocarditis infecciosa de la válvula aórtica y mitral, por
lo cual está recibiendo antibiótico con ceftriaxona y vancomicina, iniciados en
plan de completar seis semanas de tratamiento antibiótico. Se expone este caso
en particular porque es una entidad de baja frecuencia, con escasos reportes en
adultos, pero con adecuada respuesta al tratamiento antibiótico.
Palabras clave. Endocarditis, cardiopatía congénita, cirugía cardiovascular, válvulas
cardíacas, ecocardiograma.
Abstract
A
case is presented of a 33-year-old patient with a history of pulmonary
atresia-type congenital heart disease and absence of the sixth thoracic arch,
ventricular septal defect, who is hospitalized in the context of infective
endocarditis of the aortic and mitral valve, for which she is receiving
antibiotics: ceftriaxone and vancomycin, started in order to complete six weeks
of antibiotic treatment. This case is presented
because it shows a rare entity, with few reports in adults, but with an
adequate response to antibiotic treatment.
Key words. Endocarditis,
congenital heart disease, cardiovascular surgery, heart valves, echocardiogram.
ark caicyt: http://id.caicyt.gov.ar/ark:/s26184311/allpsuggx
Introducción
Las
actualizaciones en el cuidado de las cardiopatías congénitas diagnosticadas
tempranamente durante el período perinatal o en el transcurso de la infancia
hacen que un número creciente de individuos alcance altas tasas de
supervivencia, con un estilo de vida comparable con la población normal (1). Una de las tantas complicaciones de estos pacientes que
llegan a la adultez es la endocarditis infecciosa que se desarrolla comúnmente
a nivel de la válvula mitral o aórtica. Esta entidad es bien conocida en la
población pediátrica, pero no hay suficientes datos descritos en la edad adulta
(1,2).
Se
ha observado que es cada vez mayor el número de pacientes con cardiopatías
congénitas que sobreviven a través de los años, pero, a la vez, se ha descrito
un aumento en el riesgo de endocarditis infecciosa, por lo que su enfoque
terapéutico debe ser estrictamente vigilado para evitar la inestabilidad
hemodinámica y los efectos adversos tras el inicio del tratamiento (2,3).
Mediante
este reporte se presenta el caso de una mujer colombiana de 33 años
hospitalizada en el servicio de medicina interna, en conjunto con el servicio
de cardiología, la cual requirió antibioticoterapia de amplio espectro por
presentar hallazgos ecocardiográficos sugestivos de endocarditis infecciosa en
contexto de una cardiopatía congénita de base.
Caso clínico
Paciente
adulta joven de 33 años de edad con antecedente de cardiopatía congénita tipo
atresia pulmonar con ausencia del sexto arco aórtico y comunicación
interventricular, que consulta por fiebre vespertina de dos semanas de
evolución asociada a astenia y adinamia con cianosis peribucal; en el examen
físico se presenta alerta, afebril, con cianosis peribucal, en extremidades
inferiores, dedos hipocráticos con signo de vidrio de reloj, y en extremidades
superiores, dedos en palillo de tambor con signo de vidrio de reloj y cuello de
cisne (Figs. 2 y 2.1). En el examen paraclínico se observa hemograma con
policitemia (hematocrito, 71,20%, hemoglobina, 19,20 g/dl), sin leicosistosis
ni netriofilia, con proteína C reactiva elevada (37,0), con hemocultivos
negativos, y una angio-TAC de tórax que demuestra asimetría en la
vascularización pulmonar, menor en el lado izquierdo, áreas de mosaico con atenuación
en ambas bases pulmonares, engrosamiento de septos inter- e intralobulillares,
más evidentes en el pulmón izquierdo, opacidades micronodulares en el lóbulo
superior izquierdo, de localización periférica; no se identifica el tronco de
la arteria pulmonar ni ramas pulmonares confluentes; a nivel cardíaco se
aprecia cardiomegalia e hipertrofia a expensas de las cavidades cardíacas
derechas, y se observa un defecto amplio en el septo interventricular de tipo
perimembranoso compatible con comunicación interventricular de aproximadamente
31 mm de diámetro (Fig. 1). Adicionalmente, en un ecocardiograma transesofágico
se evidencia imagen de vegetaciones sobre la válvula mitral y calcificación
focal de la válvula aórtica con imagen sugestiva de pequeña vegetación en
formación. Se considera endocarditis infecciosa de válvula aórtica y mitral
junto con atresia pulmonar y comunicación interventricular por evidencia
imagenológica; se inicia esquema antibiótico con ceftriaxona y vancomicina por
seis semanas, con resultados de hemocultivos negativos; se envía a cumplir días
de antibiótico en el programa de hospitalización en casa, con buena evolución
clínica, sin complicaciones.
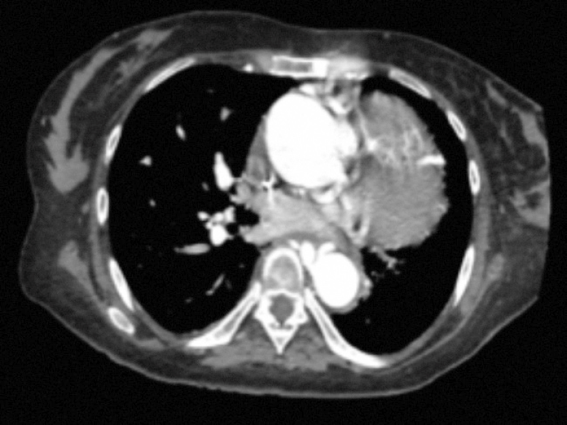
Figura 1. Angio-TAC
de tórax que muestra cardiopatía congénita tipo atresia pulmonar sin
identificación de ramas pulmonares confluyentes con comunicación
interventricular y marcada hipertrofia del ventrículo derecho, especialmente
hacia la región infundibular.
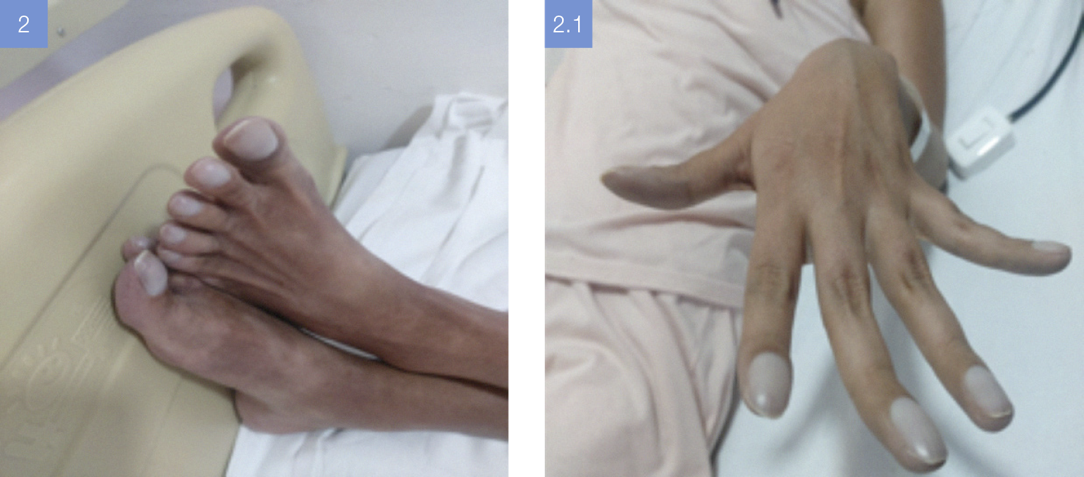
Figuras 2 y 2.1. Se
observan, en las extremidades inferiores, dedos hipocráticos con signo de vidrio
de reloj, y en las extremidades superiores, dedos en palillo de tambor con
signo de vidrio de reloj y cuello de cisne.
Discusión
La
endocarditis infecciosa es una enfermedad inflamatoria, exudativa y
proliferativa que compromete comúnmente las válvulas cardíacas aórtica y
mitral. Se asocia a menudo a la formación y aparición de estructuras
constituidas por células inflamatorias y fibrina. La evolución del cuadro
clínico se puede presentar de forma aguda, subaguda o crónica, acompañado de
fiebre de predominio vespertino principalmente (4,5). Puede haber sintomatología general inespecífica, como
astenia, adinamia, hiporexia y pérdida de peso. Entre los signos clásicos, se
encuentran manchas de Roth a nivel oftalmológico, manchas de Jenaway en las
palmas de las manos o plantas de los pies, y nódulos de Osler. Cabe mencionar
que, en estos casos, predominan como agentes causales los cocos grampositivos,
bacilos gramnegativos y hongos (5). En cuanto a los
criterios diagnósticos de la endocarditis infecciosa, tenemos la clasificación
utilizada de Von Reyn, que considera la presencia de datos clínicos, con
confirmación bacteriológica y anatomopatológica, sin tomar en cuenta datos
ecocardiográficos ni considerar la drogadicción endovenosa como factor de
riesgo. Años más tarde se desarrolló una nueva clasificación en la Universidad
de Duke, que incluyó la ecocardiografía como criterio diagnostico (6,7) (tabla 1).
|
TABLA 1.
CRITERIOS DIAGNÓSTICOS DE DUKE PARA ENDOCARDITIS INFECCIOSA |
|
|
Criterios
mayores |
Criterios
menores |
|
1. Hemocultivos positivos. - Microorganismos
típicos en dos hemocultivos separados: Streptococcus viridans, Streptococcus bovis, HACEK y Staphylococcus
aureus o bacteriemia de la comunidad por Enterococcus (los dos
últimos, sin foco primario). Según las últimas
modificaciones, también Staphylococcus spp. sin foco primario. - Microorganismo
compatible con endocarditis infecciosa aislado de hemocultivos
persistentemente positivos. - Hemocultivo único positivo para Coxiella burnetti o IgG
positiva mayor a 1:800. |
1. Factores predisponentes: enfermedad
cardíaca subyacente o uso de drogas intravenosas. |
|
2. Evidencia de compromiso endocárdico. Hallazgos
compatibles en el ECC: - Presencia de
vegetaciones. - Absceso. - Nueva dehiscencia
de la válvula protésica. - Nuevo soplo regurgitante. |
2. Fiebre mayor a 38 grados. |
|
|
3. Fenómenos vasculares: embolias
mayores, infartos sépticos pulmonares, aneurismas micóticos, hemorragia
intracraneal, hemorragia conjuntival, lesiones de Janeway. |
|
|
4. Fenómenos inmunológicos:
glomerulonefritis, nódulos de Osler, manchas de Roth, factor reumatoide
positivo. |
|
|
5. Evidencias microbiológicas:
hemocultivos positivos que no cumplen los criterios previos. |
|
|
6. Ecocardiograma sugestivo de
endocarditis infecciosa, que no cumple los criterios previos. |
|
Fuente: recuperado de García-Arribas y col.(11). Nota: Esta tabla
permite determinar los criterios basados en datos clínicos, como la presencia
de fiebre en ausencia de cultivos positivos y su asociación con datos
ecocardiográficos para, así, diagnosticar endocarditis de origen infeccioso;
se considera un caso confirmatorio si el paciente presenta un criterio mayor
y uno menor, o tres menores. ECC:
ecocardiograma; IgG: inmunoglobulina G; HACEK: Haemophilus parainfluenzae,
Haemophilus aphrophilus, Actinobacillus actinomycetemcomitans,
Cardiobacterium hominis, Eikenella corrodens y Kingella kinga. |
|
Con
respecto a la atresia pulmonar con comunicación interventricular asociada a
ausencia del sexto arco aórtico, se describe como una cardiopatía congénita
cianosante severa y poco común, que se caracteriza por la ausencia de conexión
entre el ventrículo derecho y las arterias pulmonares principalmente (8,9). El flujo hacia el territorio pulmonar
puede realizarse a través del ducto arterioso o de arterias colaterales
sistémico-pulmonares como forma de circulación colateral compensatoria. Estos
pacientes que alcanzan la adultez tienen un riesgo muy alto de desarrollar
endocarditis infecciosa, por lo que su enfoque terapéutico consiste en la
estabilización clínica inicial, la adquisición temprana de hemocultivos y el
comienzo oportuno del tratamiento médico o quirúrgico definitivo (8).
El éxito del abordaje dependerá de la elección de un antibiótico eficaz contra
el agente causal; este debe elegirse en un principio de manera empírica y
ajustarse al obtener cultivos positivos y con esto optimizar dosis terapéutica
(10).
Podemos concluir que la endocarditis infecciosa es
una patología muy prevalente pero poco estudiada en el contexto de un paciente
adulto, ya que hay poca supervivencia cuando se tiene una cardiopatía congénita
cianosante diagnosticada desde los primeros años de vida. De igual manera se
concluye que, según los criterios diagnósticos de Duke –que incluyen pruebas de
laboratorio, hallazgos ecocardiográficos, manifestaciones clínicas y factores
de riesgo–, podremos hacer diagnóstico de endocarditis infecciosa incluso en
pacientes con cardiopatías congénitas de base. En cuanto al tratamiento, se
inicia antibioticoterapia de amplio espectro ya que su patología de base
aumenta el riesgo de complicaciones y consecuentemente la muerte.
Referencias bibliográficas
1. Perich Duran RM.
Cardiopatias congenitas mas frecuentes y seguimiento en atención primaria. Pediatr Integr 2012;16:622-35
2. Cahill TJ,
Baddour LM, Habib G, et al. Challenges in infective endocarditis. J Am Coll
Cardiol 2017;69:325-44
3. Vincent LL, Otto
CM. Infective endocarditis: update on epidemiology, outcomes, and management. Curr
Cardiol Rep 2018;20
4. van den Brink R,
Lommerse I. ‘Uitbehandelen’ endocarditis kan ook oraal. Ned Tijdschr
Geneeskd 2019;163:1-10
5. Hubers SA, DeSimone
DC, Gersh BJ, Anavekar NS. Infective endocarditis: a contemporary review. Mayo Clin Proc 2020. Disponible en: https://doi.org/10.1016/j.mayocp.2019.12.008
6. Loureiro-Amigo J, Fernández-Hidalgo N, Pijuan-Domenech A y col.
Endocarditis infecciosa en adultos con cardiopatía congénita. Experiencia en un
centro de referencia. Enferm Infecc Microbiol Clin 2016. Disponible en: http://dx.doi.org/10.1016/j.
eimc.2016.01.004
7. Pérez-Lescure Picarzo J, Crespo Marcos D, Centeno Malfaz F. Guía
clínica para la prevención de la endocarditis infecciosa. An Pediatr 2014;80:3-7
8. Iung B.
Infective endocarditis. Epidemiology, pathophysiology and histopathology. Press Medicale 2019. Disponible en: https://doi.org/10.1016/j.lpm.2019.04.009
9. Olmos C, Vilacosta I, Lopez J, et al. Short-course antibiotic
regimen compared to conventional antibiotic treatment for gram-positive cocci
infective endocarditis: Randomized clinical trial (SATIE). BMC Infect Dis
2020;20:1-7
10. Hopkins MK, Dugoff
L, Kuller JA. Congenital heart disease: Prenatal diagnosis and genetic
associations. Obstet
Gynecol Surv
2019;74:497-503
11. García-Arribas D, Olmos C, Vivas D, Vilacosta I. Endocarditis
infecciosa. Med 2017;12:2380-95